Forschungsgruppe Kognition & Emotion
Menschen sind – ebenso wie Mäuse und Ratten – soziale Lebewesen. Wir lernen und verstehen unsere Umwelt nicht nur kognitiv sondern auch emotional, zum Beispiel durch Interaktionen mit anderen.
Deshalb speichern wir neben rein kognitiven Gedächtnisinhalten auch emotionale Erinnerungen, und oft sind beide Gedächtnistypen miteinander verknüpft.
Wie genau wirken Kognition und Emotion im Gehirn zusammen? Auf welche Weise gelangen Informationen über rationale Zusammenhänge und über Gefühle in die Gedächtnisstrukturen des Gehirns? Diesen Fragen ist unsere Forschungsgruppe gewidmet.
Forschungsinteressen
- Zelluläre Substrate von Hippocampus-Oszillationen beim kognitiven und emotionalen Lernen und Gedächtnis
Zelluläre Substrate von Hippocampus-Oszillationen beim kognitiven und emotionalen Lernen und Gedächtnis
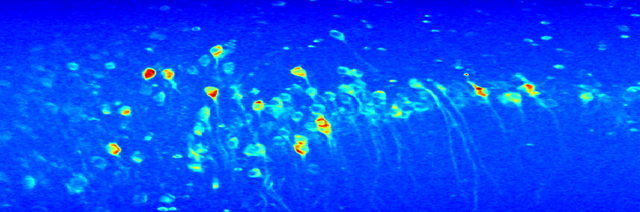
In diesem Projekt wollen wir verstehen, wie verschiedene Hippocampus-Zelltypen entlang der dorsoventralen Achse rekrutiert werden und zu Theta- und Gamma-Oszillationen während der kognitiven und emotionalen Gedächtnisbildung beitragen, wobei ein besonderer Schwerpunkt auf dem ventralen Hippocampus liegt. Während die zellulären Eigenschaften im dorsalen Hippocampus ausführlich untersucht wurden, ist uns über ventrale Hippocampus-Netzwerke wesentlich weniger bekannt. Wie sich die molekulare Vielfalt der Interneuron-Subtypen im dorsalen und ventralen Hippocampus auf ihre Funktion auswirkt, ist daher eine unserer Schlüsselfragen. Um diese Frage zu beantworten führt unsere Gruppe Kalziumbildgebung im dorsalen und ventralen Hippocampus durch, während wir mit Elektroden kontralateral entlang der dorsoventralen Hippocampusachse messen. Um die molekulare Identität der abgebildeten Zellkörper in Bezug auf Oszillationsaktivität und Verhalten aufzudecken, führen wir Expansionsmikroskopie des Gewebes durch und verwenden Algorithmen für maschinelles Lernen um die molekulare Identität mit den abgebildeten Zellkörpern abzugleichen. Die molekulare Identität wird letztendlich mit den kognitiven und emotionalen gedächtnisgesteuerten Verhaltensweisen in Verbindung gebracht.
- Gedächtnisbezogene Input-Output-Cluster von subkortikalen und hippocampalen Neuronen
Gedächtnisbezogene Input-Output-Cluster von subkortikalen und hippocampalen Neuronen
Dorsaler und ventraler Hippocampus erhalten unterschiedliche subkortikale Inputs aus Regionen wie dem medialen Septum und dem der Area Tegmentalis Ventralis, aber die funktionelle Rolle dieser Inputs ist unvollständig verstanden. Wir sind fasziniert von der Frage, wie Gradienten in der Verteilung von subkortikalen Axon- und Hippocampus-Zielzellen die Gedächtnisfunktionen beeinflussen. Um dies zu untersuchen, verwenden wir ein hochmodernes Repertoire an Methoden, um die Aktivität von Axonen und Zellpopulationen in Kombination mit Feldpotentialoszillationen entlang der dorsoventralen Hippocampusachse direkt zu messen. Auf diese Weise können wir unsere Schlüsselfrage direkt beantworten: Werden subkortikale Inputs während kognitiver und emotionaler Gedächtnisprozesse unterschiedlich rekrutiert?
- Mechanismen des sozialen Lernens und Gedächtnisses
Mechanismen des sozialen Lernens und Gedächtnisses
Um naturalistische Verhaltensweisen zu verstehen, müssen wir Bedingungen in Labor konstruieren, welche der in der Natur beobachteten Bedingungen so ähnlich wie möglich sind. Mäuse und Ratten sind wie Menschen soziale Tiere und ihre Lernprozesse werden maßgeblich von ihren Interaktionen mit Gleichaltrigen beeinflusst. Ziel dieses Projekts ist es komplexe soziale Verhaltensweisen wie Erziehung, Spiel, sexuelle Interaktion, Aggression und Kommunikation von Angst in einer Gruppe zu erkennen. Insbesondere gehen wir davon aus, dass bestimmte Schaltkreise im ventralen Hippocampus verschiedene Arten von sozialem Verhalten regulieren und mit anderen Schaltkreisen interagieren, welche der Gedächtnisbildung zugrunde liegen. Wir bauen daher „Mäuse- und Rattenstädte“, in welchen Tiere in größeren Gruppen untergebracht werden und deren Verhalten kontinuierlich überwacht wird. Wir verwenden neuartige, drahtlose Modelle von 1 Photon UCLA-Miniskopen für Bildgebung im dorsalen und ventralen Hippocampus, während wir parallel mit Elektroden messen. Dieses Projekt wird in enger Zusammenarbeit mit der Gruppe Neural Data Science unter der Leitung von Pavol Bauer (CNeu) durchgeführt.
- Leiterin

Leiterin
Sanja Bauer Mikulovic studierte Biomedizintechnik an der Technischen Universität Wien und promovierte in Neurowissenschaften an der Universität Uppsala in Schweden. Im Anschluss daran forschte sie in Schweden in der Abteilung für Neurowissenschaften als Postdoc über die Rolle spezieller Interneurontypen des Hippocampus und dessen Bedeutung für Oszillationen die kognitivem und emotionalem Verhalten zu Grunde liegen. In 2018 erhielt sie ein internationales Postdoc Grant, der ihr ermöglichte ihre Forschung parallel am Karolinska Institut in Stockholm und am Deutschen Zentrum für Neurodegenerative Erkrankungen (DZNE) in Bonn zu betreiben.
Seit Januar 2021 leitet sie ihre eigene Gruppe, die sich den Fragen wie Kognition und Emotion im Gehirn zusammenwirken, widmet.
- Team
Team
Leiterin Dr. Sanja Bauer Mikulovic +49 391 6263 93171 Sanja.Mikulovic@lin-magdeburg.de Technische Mitarbeiterinnen Daniella Hill +49 391 6263 93181 Daniela.Hill@lin-magdeburg.de PostDoc Moises dos Santos Correa +49 391 6263 93181 Moises.Correa@lin-magdeburg.de Doktoranden Anna Agafonova +49 391 6263 93181 Anna.Agafonova@lin-magdeburg.de Endre Levente Marosi +49 391 6263 93171 Endre.Marosi@lin-magdeburg.de Esmeralda Tafani Studierende Sameera Chowdhury Daniel Frias Leon Marquardt Saskia Moritz Klaus Rössel - Publikationen
Publikationen
2024
Mocellin P, Barnstedt O, Luxem K, Kaneko H, Vieweg S, Henschke JU, Dalügge D, Fuhrmann F, Karpova A, Pakan JMP, et al. 2024. A septal-ventral tegmental area circuit drives exploratory behavior. Neuron. 112(6):1020-1032.e7. https://doi.org/10.1016/j.neuron.2023.12.016
Karpova A, Aly AAA, Marosi EL, Mikulovic S. 2024. Fiber-based in vivo imaging: unveiling avenues for exploring mechanisms of synaptic plasticity and neuronal adaptations underlying behavior. Neurophotonics. 11(Suppl 1):Article S11507. https://doi.org/10.1117/1.NPh.11.S1.S11507
2023
Hilscher MM, Mikulovic S, Perry S, Lundberg S, Kullander K. 2023. The alpha2 nicotinic acetylcholine receptor, a subunit with unique and selective expression in inhibitory interneurons associated with principal cells. Pharmacological research. 196:Article 106895. https://doi.org/10.1016/j.phrs.2023.106895
2021
Mocellin P, Mikulovic S. 2021. The Role of the Medial Septum—Associated Networks in Controlling Locomotion and Motivation to Move. Front. Neural Circuits. https://www.frontiersin.org/articles/10.3389/fncir.2021.699798/full
Korvasová K, Ludwig F, Kaneko H, Sosulina L, Tetzlaff T, Remy S, Mikulovic S. 2021. Locomotion induced by medial septal glutamatergic neurons is linked to intrinsically generated persistent firing. BioRxiv. https://doi.org/10.1101/2021.04.23.441122
Sarkar I, Maji I, Omprakash C, Stober S, Mikulovic S, Bauer P. 2021. Evaluation of deep lift pose models for 3D rodent pose estimation based on geometrically triangulated data. CV4Animals Workshop, CVPR 2021. https://arxiv.org/abs/2106.12993
2019
Hilscher MM, Nogueira I, Mikulovic S, Kullander K, Leao RN, Leao KE. „Chrna2-OLM interneurons display different membrane properties and h-current magnitude depending on dorsoventral location” Hippocampus. 2019. 10.1002/hipo.23134 https://onlinelibrary.wiley.com/doi/full/10.1002/hipo.23134
Çalışkan G, Mikulovic S, Girardeau G. 2022. Editorial: Functional Aspects of Mesoscopic Brain Oscillations: Insights From in vivo and in vitro Studies. Frontiers in neural circuits. 16:Article 960157. https://doi.org/10.3389/fncir.2022.960157
2018
Mikulovic S, Restrepo CE, Siwani S, Bauer P, Pupe S, Tort AB, Kullander K, Leao RN. “Ventral hippocampal OLM cells control type 2 theta oscillations and response to predator odor.” Nature Communications. 2018; 9(1):3638. https://www.nature.com/articles/s41467-018-05907-w
Siwani S, Franca ASC, Mikulovic S, Reis A, Hilscher MM, Edwards SJ, Leao RN, Tort AB, Kullander K, Leao RN. “OLMα2 Cells Bidirectionally Modulate Learning.” Neuron. 2018; 99(2):404-412.e3. https://doi.org/10.1016/j.neuron.2018.06.022
Winne J, Franzon R, De Miranda A, Malfatti T, Patriota J, Mikulovic S, Leao KE, Leao RN. “Salicylate induces anxiety-like behavior and slow theta oscillation and abolishes the relationship between running speed and fast theta oscillation frequency”. Hippocampus. 2018; 0.1002/hipo.23021. 10.1002/hipo.23021
Bauer P, Engblom S, Mikulovic S, Senek A. “Multiscale modelling via split-step methods in neural firing”. Mathematical and Computer Modelling of Dynamical Systems. 2018; 10.1080/13873954.2018.1488740. https://doi.org/10.1080/13873954.2018.1488740
2016
Mikulovic S, Pupe S, Maia Peixoto H, Nascimiento G, Kullander K, Tort AB, Leao RN. “On the photovoltaic effect in local field potential recordings.” Journal of Neurophotonics. 2016; 3(1):015002. 10.1117/1.NPh.3.1.015002
2015
Mikulovic S, Restrepo CE, Hilscher MM, Kullander K, Leao RN. “Novel markers for OLM interneurons in the hippocampus.” Frontiers in Cellular Neuroscience. 2015; 2;9:201.
2014
Arvidsson E, Viereckel T, Mikulovic S, Wallén-Mackenzie Å. “Age- and sex-dependence of dopamine release and capacity for recovery identified in the dorsal striatum of C57/Bl6J mice.” PLoS One. 2014; 9(6):e99592.
2013
Zelano J, Mikulovic S, Patra K, Kuehnemund M, Larhammar M, Emilsson L, Leao RN, Kullander K. ”The synaptic protein encoded by the gene Slc10A4 suppresses epileptiform activity and regulates sensitivity to cholinergic chemoconvulsants.” Journal of ExperimentalNeurology. 2013; 239:73-81
2012
Leao RN, Mikulovic S, Leao KE, Munguba H, Gezelius H, Enjin A,Patra K, Eriksson A, Loew LM, Tort AB, Kullander K. “OLM interneurons differentially modulate CA3 and entorhinal inputs to hippocampal CA1 neurons.” Nature Neuroscience. 2012; 15(11):1524-30.
Enjin A, Leao KE, Mikulovic S, Le Merre P, Tourtellotte WG, Kullander K. “Sensorimotor function is modulated by the serotonin receptor 1d, a novel marker for gamma motoneurons.” Journal of Molecular and Cellular neuroscience. 2012; 49(3):322-32.